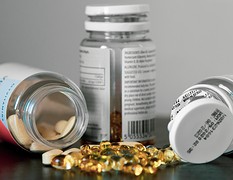
L'industria farmaceutica e le sfide del confezionamento
L'industria del packaging farmaceutico nel 2025 continua ad affrontare le sfide di un mercato che cresce e cambia composizione tra spinta regolatoria, nuovi materiali e fabbriche intelligenti.
A cura di Riccardo Ceredi
Nel 2025 il packaging farmaceutico continua a espandersi, ma non in modo uniforme e, soprattutto, non secondo una sola metrica. Secondo Fortune Business Insights, il valore globale del comparto è stimato in 116,58 miliardi di dollari, con una traiettoria che lo porterà a 177,12 miliardi entro il 2032. La leadership rimane saldamente in Nord America, un mercato che da solo rappresenta circa il 30% del complessivo, trainato da consumi elevati, da forti investimenti in ricerca e dallo sviluppo accelerato di terapie biologiche e iniettabili.
Ma le dinamiche sono globali e investono tanto i mercati emergenti, con un consumo di farmaci in forte crescita, quanto i Paesi europei, dove il packaging è al centro di un intenso lavoro di innovazione tecnologica e di adattamento alle normative. In parallelo, i report settoriali proiettano un raddoppio del sotto-mercato statunitense entro il 2034, con un ruolo dominante del primario – siringhe, flaconi, cartucce – e delle tecnologie “smart”. Questi trend stanno già incidendo in profondità sulle tecnologie di processo e confezionamento e i costruttori sono chiamati a ripensare standard, specifiche e materiali in risposta a un’industria che evolve con una rapidità senza precedenti.
La spinta regolatoria: Europa e Stati Uniti
Nel 2025 l’Europa è uscita dalla fase negoziale e ha reso vincolante il nuovo Regolamento sugli imballaggi e i rifiuti da imballaggio (PPWR, Packaging and Packaging Waste Regulation). Il testo è entrato in vigore l’11 febbraio 2025 e, salvo eccezioni, si applicherà dopo 18 mesi. Gli obiettivi fissati toccano l’intero ciclo di vita del packaging: riduzione degli imballaggi superflui, riciclabilità totale entro il 2030, incremento del contenuto riciclato “sicuro” e armonizzazione dei diversi sistemi nazionali di gestione dei rifiuti. Per il farmaceutico, tradizionalmente considerato un settore speciale in materia di materiali, significa progettare imballaggi e linee produttive compatibili con criteri di riciclabilità, senza però derogare a requisiti imprescindibili come sterilità, barriera e integrità del farmaco.
Sul fronte della tracciabilità rimane in vigore la Direttiva europea sui medicinali falsificati (FMD, Falsified Medicines Directive), che impone l’apposizione di elementi di sicurezza obbligatori: un identificativo univoco in codice DataMatrix bidimensionale e un dispositivo anti-manomissione. Negli Stati Uniti, intanto, è arrivata a maturità la Drug Supply Chain Security Act (DSCSA). Dal 2024 tutta la filiera farmaceutica deve adottare sistemi elettronici e interoperabili per la tracciabilità delle confezioni individuali, con aggiornamenti normativi e linee guida operative introdotte nel 2025. In termini pratici, ciò significa che le macchine devono poter dialogare con i sistemi di serializzazione e con le banche dati lungo l’intera catena di fornitura, dall’aggregazione delle confezioni fino al loro ultimo passaggio logistico.
Materiali e sicurezza: tra vetro, polimeri ad alte prestazioni e catena del freddo
Il vetro resta il materiale di riferimento per molti farmaci iniettabili, ma la crescita delle terapie biologiche e di formulazioni complesse sta aprendo spazio a soluzioni alternative. In particolare, i polimeri ciclici come il COP (polimero olefinico ciclico) e il COC (copolimero ciclico olefinico) vengono sempre più utilizzati per flaconi e siringhe. Rispetto al vetro, questi materiali garantiscono maggiore resistenza alla rottura, tolleranze dimensionali più stabili e interazioni superficiali meglio controllabili. COP e COC, pur simili, presentano differenze significative: il primo è spesso scelto per la sua robustezza meccanica, il secondo per la trasparenza ottica, in base alle caratteristiche del principio attivo da contenere. Parallelamente, l’espansione di farmaci sensibili alla temperatura – come vaccini a mRNA, terapie cellulari e geniche, prodotti biologici – sta spingendo la domanda di soluzioni per la catena del freddo. Il mercato del packaging destinato a mantenere condizioni termiche controllate cresce a doppia cifra a livello globale, con l’Europa tra le aree di maggiore incidenza. A questo scenario si aggiunge la cornice normativa: il PPWR indirizza il comparto verso un utilizzo sicuro di materiali riciclati e monomateriali. Nel farmaceutico, però, questa transizione richiede valutazioni molto più stringenti rispetto ad altri settori, in particolare sul fronte della compatibilità chimica, della migrazione dei materiali e della sterilità.
Siringhe pre-riempite, cartucce e autoiniettori: il primario che accelera
Nel panorama del packaging farmaceutico, le siringhe pre-riempite sono oggi tra i formati più dinamici. La loro diffusione è legata a due fattori principali: da un lato l’espansione delle terapie biologiche, spesso somministrate in dosaggi precisi e sensibili, dall’altro la crescente richiesta di soluzioni pensate per l’autosomministrazione, che permette ai pazienti di gestire direttamente i trattamenti a domicilio, riducendo la pressione sulle strutture sanitarie.
Accanto alle siringhe, stanno crescendo anche le cartucce per penne e gli autoiniettori, dispositivi che uniscono farmaco e sistema di somministrazione in un’unica soluzione. La spinta più evidente arriva dalle terapie utilizzate nel trattamento del diabete di tipo 2 e oggi in rapida estensione anche nell’ambito della cura dell’obesità. Le proiezioni di mercato indicano per queste famiglie tassi di crescita a doppia cifra fino al 2030, con un valore globale che supererà gli attuali 8-9 miliardi di dollari già nel breve periodo.
Per il settore del packaging questo significa affrontare sfide complesse: garantire riempimento asettico sempre più sofisticato, introdurre sistemi avanzati di controllo visivo per ogni singola unità e assicurare livelli di sicurezza del dispositivo tali da prevenire incidenti o manomissioni. Questa tendenza ha anche un riflesso sul confezionamento secondario, dove cresce l’attenzione verso soluzioni con tamper evidence, sistemi di protezione dell’ago e, sempre più spesso, strumenti di tracciabilità nativa che accompagnano ogni dose lungo l’intera filiera.
In questo senso, i formati in rapida espansione rappresentano non solo un’opportunità commerciale, ma anche un banco di prova tecnologico che costringe i costruttori di macchine a ripensare standard, architetture e materiali in modo coerente con l’evoluzione del farmaco e delle abitudini di cura.
(...)
L'articolo completo è contenuto nel numero di Ottobre di Rassegna dell'imballaggio,
Gallery